
قلع؛ سمی اما بی خطر
مروری بر خواص قلع
قلع عنصری شیمیایی است که در زبان انگلیسی با نام Tin و در زبان لاتین به نام Stannum شناخته می شود. به همین دلیل است که امروزه آن را با علامت اختصاری Sn می شناسیم. این عنصر 49 امین عنصر فراوان پوسته زمین شناخته می شود. این بدان معنی است که حدود 0/001% سهم پوسته زمین مخصوص به این فلز است. استحصال این فلز از سنگ معدن کاسیتریت (cassiterite) انجام می شود که حاوی ترکیبات اکسیدی قلع است.
قلع 50 امین عنصر جدول تناوبی فلزات است. فلزی که در گروه چهاردهم جدول تناوبی هم گروه با نافلزاتی چون کربن، سیلیسیم و ژرمانیوم شده است. بنابراین انتظار می رود که به لحاظ خواص شیمیایی، تا حدودی با این عناصر شباهت داشته باشد.
تاریخچه کشف و استفاده از این فلز، به هزاران سال پیش برمی گردد. در اصل، برنز که به عنوان یکی از مهم ترین آلیاژها در متالورژی و ریخته گری شناخته می شود، بر پایه عناصر مس و قلع است که از 3000 سال پیش از میلاد مسیح مورد استفاده قرار می گرفت و آغازگر عصری به نام عصر برنز شد. پس از برنز، آلیاژهای بسیاری از بر پایه قلع و عناصر دیگر توسعه یافتند که از جمله معروف ترین آن ها می توانیم به مسوار، لحیم، ورقه ها و روکش ها اشاره کنیم.

خواص فیزیکی
قلع فلزی نرم، چکش خوار و انعطاف پذیر است که رنگی بین ما بین سفید و نقره ای دارد. این عنصر در میان عناصر فلزی نقطه ذوب پایینی دارد و تنها در 232 درجه سانتیگراد ذوب می شود. در بین عناصر گروه 14 نیز قلع کمترین نقطه ذوب را دارد.
در حالت معمول، قلع دو ساختار دگرشکل (آلوتروپ) دارد:
- قلع β که به نام قلع سفید معروف است. این آلوتروپ ساختار تتراگونال مرکزدار BCT دارد و در دمای بالاتر از 13.2 درجه سانتیگراد پایدار است. قلعی که برای کاربردهای معمول استفاده می شود؛ از این نوع است.
- قلع α که به نام قلع خاکستری معروف است و در دماهای زیر 13.2 درجه سانتیگراد پایدار است. این دگرشکل همانند الماس، سیلیسیوم و ژرمانیوم ساختار کریستالی مکعبی کریستالی (DC) دارد، به شدت ترد بوده و کاربرد بسیار محدودتری نسبت به نوع β دارد.
دقت داشته باشید که این دما برای حالتی است که فلز قلع خالص باشد. در صورتی که هر گونه ناخالصی مانند مس، نفره، آنتیوموان، کادمیم یا بیسموت به این عنصر اضافه شود و تشکیل محلول جامد بدهد، دمای استحاله افت کرده و به زیر 0 درجه می رسد. به همین دلیل عملا برای کاربردهای متداول، تنها ساختار کریستالی β است که کاربرد دارد.
خواص شیمیایی
قلع از لحاظ مقاومت خوردگی، فلزی در رده متوسط محسوب می شود. این فلز در برابر حملات خوردگی توسط آب مقاومت می کند، اما در برابر اسیدها و بازهای قوی مورد حمله قرار گرفته و تخریب می شود. این فلز را می توان جلا داده و به عنوان لایه ای محافظ برای محافظت سایر فلزات استفاده کرد. این فلز با تشکیل لایه پسیو (Passive Layer) از خورده شدن فلز در محیط جلوگیری می کند.
قلع در شرایط محیطی 10 ایزوتوپ پایدار دارد که در نوع جالب محسوب می شود. این عنصر بیشترین ایزوتوپ های پایدار را در بین عناصر جدول تناوبی دارد. این ایزتوپ ها با عدد جرمی 112، 114، 115، 116، 117، 118، 119، 120، 122 و 124 در طبیعت یافت می شوند. ایزوتوپ های 116، 118 و 120 فراوان ترین ایزوتوپ های این عنصر هستند که در میان آن ها 120Sn جایگاه ویژه ای دارد. چرا که در بین روش های آنالیز مولکولی مثل آنالیز NMR به راحتی شناسایی می شود.
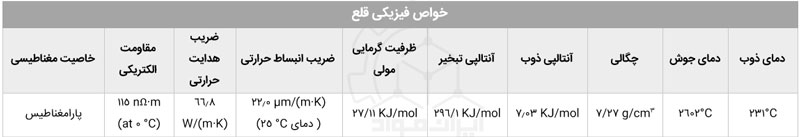
به علاوه، تاکنون 31 ایزوتوپ ناپایدار از این عنصر شناسایی شده است که گستره ای از 99 تا 139 دارند. در بین این ایزوتوپ ها، 126Sn با 230000 سال بیشترین نیمه عمر را دارد. باقی ایزوتوپ های قلع نیمه عمری کمتر از یک سال دارند. در جدول زیر می توانید خواص شیمیایی مربوط به این فلز را مشاهده کنید.

قلع به چه صورتی تولید می شود؟
استحصال قلع از سنگ های معدنی در دو مرحله انجام می شود. برای بیشتر کانی هایی که شامل فلزاتی مثل کروم، آهن، نیکل، سرب و قلع می شوند، مرحله اول تهیه کنسانتره ای است که متشکل از کانی های فلزی است. در این مرحله کانی های زائد با روش های مختلف جداسازی شده و دور ریخته می شوند. این فرایند به نام فرایند تغلیظ معروف است. پس از تغلیظ، کنسانتره ای که عمدتا شامل ترکیبات اکسیدی است، در کوره حرارت داده می شود تا احیا شود. پس از این مرحله مذابی از قلع به دست می آید که حاوی ناخالصی است. در مرحله آخر خالص سازی توسط فرایند الکترولیز انجام می شود که خلوص فلز را تا 99/96% بالا می برد.
در این قسمت توجه شما را به فیلم کوتاهی که در خصوص معرفی این فلز محبوب تهیه شده، جلب می کنیم.
کاربردهای قلع
قلع با توجه به خصوصیات فیزیکی و شیمیایی منحصر به فردی که دارد، توانسته به خوبی جای خود را در صنایع باز کند. کاربردهای این فلز بیشتر در تماس با فلزات دیگر و آلیاژسازی با آن ها نمود پیدا می کند. در این قسمت به مهم ترین استفاده های این فلز اشاره می کنیم:
لحیم کاری
لحیم آلیاژی ترکیبی از قلع و سرب با نسبت های متغیر بین 5 تا 70 درصد وزنی قلع است که برای اتصال دو یا چند فلز استفاده می شود. در صورتی که نسبت قلع و سرب لحیم در حدود 63 و 37 درصد وزنی باشد، این آلیاژ پایین ترین نقطه ذوب را خواهد داشت. به همین همین دلیل معمولا از نسبت وزنی حدود 60 به 40 در ساخت سیم های لحیم استفاده می شود و سیم لحیم با این ترکیب شناخته شده است.

روکش فلزات
حتما تاکنون با ظروف مسی سر و کار داشته و درون آن ها را دیده اید. این پوشش از فلز قلع است که از خورده شدن فلز مس در تماس با غذا جلوگیری می کند. زیرا مس در معرض رطوبت به مرور زنگ زده و ترکیبات اکسیدی آن وارد غذا می شود که بسیار سمی و خطرناک است. این فلز به خوبی با سطوح فلزاتی مانند آهن، سرب، روی و فولاد پیوند برقرار می کند و با ایجاد لایه ای چسبنده از سطوح آن ها محافظت می کند. به همین دلیل است که درون قوطی های کنسرو مواد فلزی با لایه ای از قلع پوشش داده شود تا مواد غذایی به مدت طولانی قابل نگه داری باشند.

ساخت آلیاژهای خاص
این فلز در ترکیب با سایر عناصر محدوده وسیعی از آلیاژهای صنعتی را تولید می کند. معروف ترین آلیاژ این عنصر برنز (مفرغ) است که از ترکیب این فلز با مس تولید می شود. در صورتی که مقداری فسفر به این ترکیب اضافه شود، برنز فسفری (Phosphor bronze) ایجاد می شود.
مسوار (pewter) یکی دیگر از آلیاژهای مهم قلع است که بین 85-99% قلع دارد. این آلیاژ جزو آلیاژهای گران قیمت قلع به حساب می آید و به صورت مفتول، لوله و … در بازار عرضه می شود. بیشترین کاربرد این آلیاژ در ساخت وسایل آشپزخانه و وسایل تزئینی است.
سیم مفتول (Wire)
در بین سیمهای فلزی، سیم مفتول یکی از پرکاردبرترین سیمها است که کاربردهای زیادی...این فلز به دلیل قیمت پایین تر، سهولت ساخت و خواص بهتر در برخی موارد گوی سبقت را از آلومینیوم ربوده است و در ساخت ورقه ها، مخازن و شمش ها جایگزین آلومینیوم شده است.
ساخت کاتالیزورها
زمانی که در محیط اکسیژن وجود داشته باشد، قلع وارد عمل شده و به واکنش های شیمیایی را تسریع می کند. از این ویژگی در ساخت کاتالیزور استفاده می شود.
صنعت نساجی
مهم ترین ترکیب قلع، کرید این فلز یا ترکیب شیمیایی SnCL4 است. از این ترکیب در صنعت چاپ روی پارچه استفاده می شود که به عنوان یک عامل کاهنده و خورنده عمل می کند. هم چنین این فلز در تولید رنگ های چاپی نیز کاربرد دارد.

ساخت ابررساناها
جالب است بدانید که یک ابررسانای مغناطیسی با وزن تنها 2 کیلوگرم قادر است میدان مغناطیسی برابر با یک آهنربای الکترومعناطیسی چند تنی ایجاد کند. این موضوع اهمیت استفاده از استفاده از ابررسانا را بیش از پیش برای ما مشخص می کند. قلع در ترکیب با فلز نیوبیوم (Nb) تشکیل ترکیب Nb3Sn می دهد که ترکیبی رایج در ساخت آهنزباهای ابررسانا است.
صنعت پلیمر
بدون شک اگر با پلیمرها آشنایی داشته باشید، پلی وینیل کلراید (PVC) را به عنوان یکی از پرکاربردترین پلاستیک ها در صنعت پتروشیمی می شناسید. این پلیمر ارزان بوده و به راحتی سر هم بندی می شود. به همین دلیل در سال های اخیر جایگزین بسیاری از مصالح ساختمانی در ساختمان سازی شده است. اما جالب است بدانید بدون حضور قلع به عنوان تثبیت کننده، این پلیمر به سرعت فاسد و غیر قابل مصرف می شود.
سرامیک ساختمانی
به حال دقت کرده اید با هر بار نگاه کردن به اطراف خود در خانه، محل کار، معابر عمو...شیشه سازی
شاید اصطلاح شیشه شناور یا پیلکینگتون (Pilkington) به گوشتان خورده باشد. امروزه اکثر پنجره های جدید با شیشه های رفلکس، شیشه های ایمنی یا خود تمیز شونده (Self-Cleaning) از این نوع تهیه می شوند. این نوع شیشه ها توسط شیشه مذاب شناور بر روی بستری از فلز مذاب قلع تولید می شوند.
کلرید این فلز با پاشیده شدن بر روی سطوح شیشه ای لایه ای با خاصیت هدایت الکتریکی ایجاد می کند. از این پوشش ها در شیشه های اتومبیل ضد یخ و روشنایی تابلو فرمان استفاده می شود.

ذخایر قلع در ایران و جهان
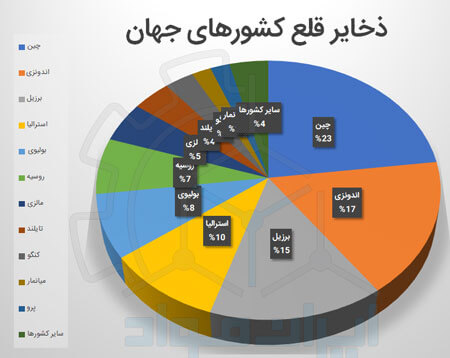
ذخایر قطعی که تاکنون از این فلز برآورد شده است، حدود 4 میلیون و 700 هزارتن تخمین زده شده است که بیشترین ذخایر این فلز معدنی مربوط به آسیا و به خصوص کشورهای آسیای شرقی است. جایی که چین با 23% بیشترین ذخایر معدنی این فلز را در جهان دارد. بر اساس اطلاعات سازمان زمین شناسی ایالات متحده آمریکا، ذخایر قطعی این کشور تا سال 2019 حدود 1 میلیون و 100 هزارتن تخمین زده شده است. پس از این کشور، اندونزی، برزیل، استرالیا، بولیوی، روسیه و مالزی عمده ذخایر این فلز را در جهان در اختیار دارند.
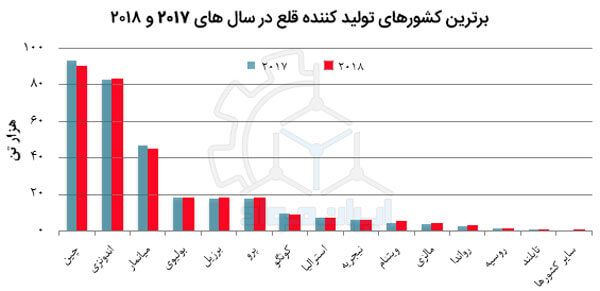
تولید این فلز از محصولات بازیافتی بسیار رایج است. به گونه ای که امروزه بین 15 تا 19 درصد این فلز از منابع بازیافتی و قراضه ها تامین می شود و باقی آن از تولیدات معدنی تامین می شود. چین به عنوان کشوری که بیشترین ذخایر را در اختیار دارد، بیشترین میزان تولید جهان را هم در اختیار دارد. این کشور با تولید 90 هزار تن قلع در سال 2018، حدود 29% تولید جهانی به خود اختصاص داد. پس از آن کشورهای اندونزی، میانمار، بولیوی و برزیل بیشترین مقدار تولید جهانی را به خود اختصاص داده اند. در جدول زیر می توانید میزان تولید کشورهای مختلف را در سال های 2017 و 2018 ملاحظه کنید.
در کشور ما نیز چند نقطه به لحاظ بهره وری از ذخایر قلع تاکنون شناسایی شده اند. معادن شاه کوه در شرق کشور، معادن تربت حیدریه در خراسان، معدن چاه پلنگی در نزدیکی اصفهان، معدن انجرد در آذربایجان شرقی و تیژ تیژ در سنندج از جمله مناطقی هستند که ذخایری از این فلز را در خود دارند.
در هنگام استفاده از قلع احتیاط کنید!
شاید تصور کنید که قلع فلزی کاملا بی خطر است و برای سلامت انسان مشکلی ایجاد نمی کند. اما در صورتی که مقدار این فلز از حد مجاز بیشتر شود، سلامت انسان را با خطر جدی مواجه می کند. عوارض کوتاه مدت آن شامل سوزش و سوختگی چشم و پوست، سرگیجه، تنگی نفس و درد در اندام های مختلف و اثرات مزمن آن به صورت تضعیف سیستم ایمنی، آسیب به اندام های مختلف از جمله کبد و افسردگی می شود. بنابراین سعی کنید از مصرف بیش از حد غذاهای کنسروی یا خوردن مداوم غذا درون پوشش داده شده با قلع خودداری کنید.
برای دریافت فایل ها با گوشی همراه، دکمه دانلود را برای چند لحظه فشرده و در یک صفحه جدید فایل مربوطه را دانلود نمایید.
پسورد فایل فشرده : www.iran-mavad.com





















دیدگاه کاربران
با سلام لینک دانلود مشکل دارد دانلود نمیشود.لطفا بررسی کنید