
سولفوریک اسید (جوهر گوگرد)
«سرانۀ مصرف یک مادۀ شیمیایی به ازای هر فرد، معیار پیشرفت یک کشور است!» مطمئنا در نگاه اول گمان می کنید این یک جملۀ نادرست است؛ اما اینطور نیست. این جمله دربارۀ اسید سولفوریک صحبت می کند. یکی از مهم ترین مواد شیمیایی جهان که لقب سلطان مواد شیمیایی را دارد. در صورتی که قصد خرید این اسید معدنی را دارید و یا می خواهید در مورد آن اطلاعاتی به دست آورید، پیشنهاد می کنیم مطالعهی این مقاله را از دست ندهید.
آشنایی اولیه با اسید سولفوریک
سولفوریک اسید (جوهر گوگرد) یک اسید معدنی بسیار سوزاننده با فرمول شیمیایی H2SO4 است. این اسید دارای خاصیت خورندگی بر روی فلز، بافت های زنده و حتی سنگ است؛ بنابراین در زمرۀ مواد خطرناک قرار می گیرد. از نظر فیزیکی نیز به صورت مایعی رقیق، بی رنگ و کاملا محلول در آب است.
سولفوریک اسید دارای مولکول هایی قطبی است که می توانند با یکدیگر پیوند هیدروژنی برقرار کنند. بنابراین نقطه جوش بالا و ویسکوز بودن آن توجیه می شود. همین شرایط مولکولی است که باعث می شود H2SO4 به خوبی در آب حل شود و محلول های اسیدی مختلفی را تولید کند.
تاریخچۀ تولید سولفوریک اسید
تاریخچهی کشف و تولید جوهر گوگرد نشان میدهد که دانشمندان مسلمان ایرانی در این زمینه نیز پیشتاز بودهاند. جابر ابن حیان، پدر علم شیمی، نخستین کسی بود که توانست از اختلاط مواد شیمیایی سولفوریک اسید را تولید کند. در شکل زیر روند پیشرفت تولید این اسید را تا زمان تجاری شدن آن ملاحظه میکنید.

مشخصات فنی و خواص جوهر گوگرد
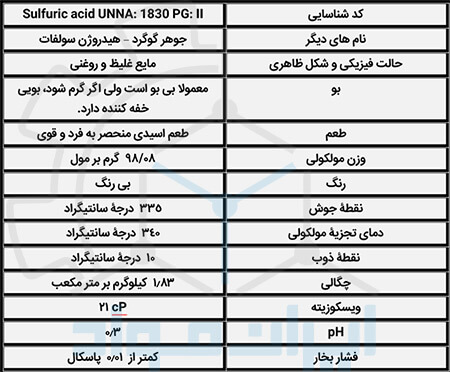
مراحل تولید H2SO4
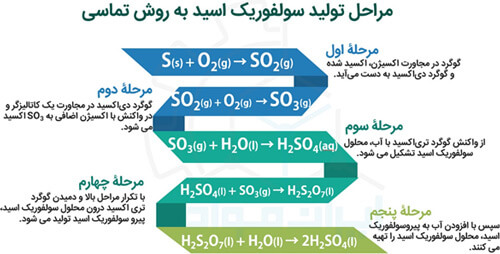
اصلی ترین روش تولید جوهر گوگرد، روش تماسی یا مجاورت است که در شکل زیر به خوبی مراحل آن بیان شده است:
کاربردهای جوهر گوگرد
همان طور که پیش از این ذکر شد، این اسید یکی از مهم ترین مواد شیمیایی و آزمایشگاهی است تا جایی که می توان دربارۀ کاربردهای این ماده شیمیایی چندین جلد کتاب نوشت! در این مطلب به طور خلاصه به برخی از مهمترین کاربردهای این اسید اشاره ای خواهیم داشت.
کاربرد در اصلاح خاک
جوهر گوگرد در تولید مواد اصلی کودهای شیمیایی به کار می رود. کودهایی مانند اسید فسفریک، سولفات آمونیوم و سوپرفسفات نرمال به صورت مستقیم از این اسید معدنی تولید می شوند. همچنین بخش اندکی از این اسید به طور مستقیم در مخلوط کودهای مایع مورد استفاده قرار می گیرد.
با اضافه کردن ایت اسید معدنی به آب آبیاری واکنشی با کربنات کلسیم موجود در خاک برقرار می شود که نتیجهی آن تولید سولفات کلسیم آب دار یا همان «گچ کشاورزی» است. گچ خامی که به سطح خاک اضافه می شود با گچ حاصل از واکنش اسید با آهک موجود در خاک تفاوت دارد. سولفوریک اسید در مقایسه با گچ خام، سرعت تاثیر بالایی در بهبود خواص خاک دارد.
کاربرد در استخراج مس
یکی از روش های مهم استخراج مس فرآیند هیدرومتالورژی است. اساس این فرایند بر پایۀ به کارگیری سنگ کانی های سولفیدی و اکسیدی مس است که در روش لیچینگ (Leaching) اتفاق می افتد. در این روش برای انحلال مس از اسیدهای قوی مثل H2SO4 استفاده می کنند که مراحل استخراج با حلال و الکترووینینگ (Electrowining) در ادامه آن قرار دارد. لیچینگ مس در نتیجه حل شدن مس موجود در کانههای آن در یک محلول آبی اتفاق می افتد که این محلول اغلب اسید رقیق است.
کاربرد در صنایع آهن و فولاد
این اسید در صنایع آهن و فولاد دو کاربرد عمده دارد. یکی بازیافت گازهای حاوی آمونیاک که منجر به تولید سولفات آمونیوم به عنوان محصول جانبی صنعت فولاد می شود. دیگری رسوب زدایی که شامل زدودن اکسیدهای فلزات، چربی ها و نمک ها از روی سطح فولاد می شود.
کاربرد در سنتز مواد شیمیایی
یکی از مواد اساسی برای راه اندازی یک آزمایشگاه شیمی سولفوریک اسید است. از این اسید میتوان در تولید مواد شیمیایی مختلفی استفاده کرد که برخی از آنها عبارتند از:
- تولید اسید بوریک از H2SO4 و بورات سدیم
- تولید اسید سیتریک از H2SO4 و سیترات کلسیم
- تولید اسید کلریدریک از H2SO4 و نمک طعام
- ساخت اسید کرومیک و انواع بی کرومات ها
- سنتز دی اکسید تیتانیوم با فرایند سولفاته کردنپ
- تولید متیل متاکریلات از روش استو سیانو هیدرین
- تولید کاپرولاکتام و تولید محصول جانبی سولفات آمونیوم
- و…
کاربرد در مواد منفجره
حتما نام نیتروگلیسیرین (C3H5N3O9) به گوشتان خورده است. یک ماده منفجره بسیار قوی با اثرات تخریبی بالا و یکی از پر استفادهترین اجزای ترکیبی برای مواد منفجره تجاری. نیتروگلیسیرین از تزریق گلیسیرین بسیار غلیظ به داخل محلول بسیار غلیظ اسید نیتریک و اسید سولفوریک تهیه می شود.
کاربردهای غیرآزمایشگاهی نیتروگلیسیرین بسیار محدود است. این ماده فقط به صورت محلول در حلال های غیرمنفجره یا مخلوط با مواد بی اثر پودری که حاوی بیش از ۰٫۵ درصد نیتروگلیسیرین نباشد، مجوز حمل و نقل دارد. البته امروزه از نیتروگلیسیرین در مواد منفجره نظامی استفاده نمی شود و از آن فقط در پیشرانه های موشک ها استفاده می شود.
کاربرد در صنایع دیگر
اسید سولفوریک در صنایع دیگری نیز کاربرد دارد:
- در فرایند تولید کلر از روش سل های دیافراگمی
- در بعضی واحدهای پودر و مایع شوینده جهت سولفوناسیون و تولید محلول چربی گیر و باز کننده
- در کارخانجات روغن نباتی برای زدودن چربی از ماشین آلات
- در صنعت نساجی برای تثبیت رنگ پارچه و نخ
- در صنعت چرم سازی برای زدودن چربی از چرم خام
- در صنعت کاغذ جهت کنترل pH و تصفیه کاغذ و زدودن ناخالصی های معدنی
- در ضد عفونی کردن لوله فاضلاب و شستشوی کاشی و سرامیک
- جذب آب در تولید میوه خشک
- و…
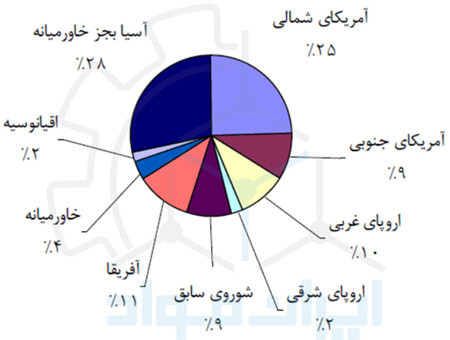
شکل زیر سهم تولید H2SO4 در هر یک از مناطق عمده جهان را نشان می دهد.
نکات ایمنی در هنگام استفاده از H2SO4
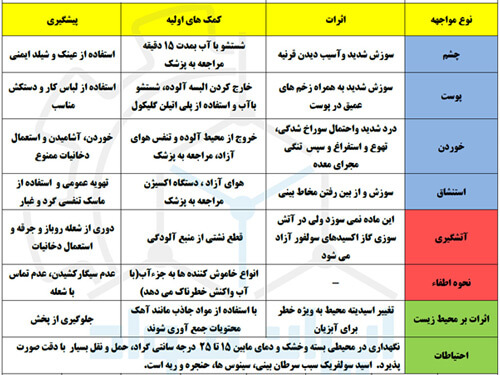
در استفاده از اسید سولفوریک ، آگاهی از روش مواجهه با اتفاقات احتمالی و رعایت نکات ایمنی ضروری است. در جدول زیر اثرات برخورد این اسید با اعضای بدن یا محیط زیست، کمک های اولیه و روش های پیشگیری آورده شده است.
عوامل موثر بر قیمت اسید سولفوریک
عمده تولید H2SO4 در جهان، از گوگرد عنصری است. سهم این عنصر از تأمین اسید در سال ۲۰۱۳، برابر با ۵۹ درصد بود که اختلاف قابل توجهی با منابع دیگر اسید دارد. تولید سولفوریک اسید از گازهای خروجی واحدهای ذوب فلزات نیز مرسوم است که سهمی برابر با ۲۹ درصد دارد.
قیمت اسید در شهرها و استان های مختلف، متفاوت است. علت اصلی این تفاوت قیمت، به میزان دسترسی به واحدهای ذوب محلی باز می گردد. بیشتر بازارهای محلی فروش اسید در اطراف واحدهای ذوب فلزات پایه تشکیل شده و هزینههای حمل و نقل از نزدیک ترین واحد ذوب، اثرات مهمی در قیمت این اسید دارد. در نقاطی که کارخانجات ذوب فلزات وجود نداشته باشد، قیمت جوهر گوگرد عمدتاً توسط قیمت گوگرد خالص تعیین می شود.
منابع
استاندارد MSDS CODE: AD4221
انتشارات شرکت پالایش و پخش (۱۳۸۹)- اسید سولفوریک و خطرات آن


















دیدگاه کاربران