
منیزیم ؛ سبک ترین فلز سازه ای جهان
منیزیم یک عنصر شیمیایی با نماد Mg و عدد اتمی 12 است. این فلز جامد، ظاهری خاکستری و براق دارد که شباهت ظاهری زیادی به پنج عنصر دیگر در گروه دوم جدول تناوبی دارد. می دانیم که همه عناصر گروه 2 (عناصر قلیایی خاکی) دارای پیکربندی الکترونی یکسان در پوسته بیرونی و ساختار بلوری مشابهی هستند.
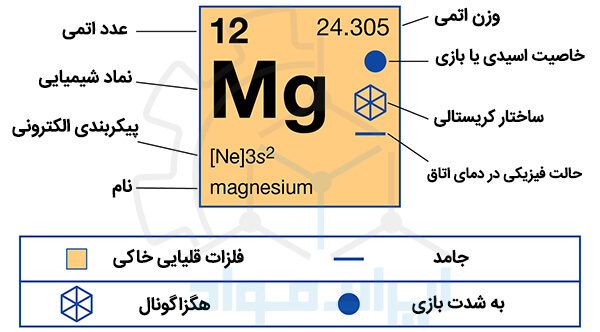
منیزیوم هشتمین عنصر فراوان در جهان است. این عنصر فلزی در ستاره های بزرگ و پیر از پیوستن سه هسته هلیوم به یک هسته کربن یا به هم پیوستن هلیوم و نئون تولید می شود. وقتی چنین ستاره هایی به عنوان ابرنواختر (supernova) منفجر می شوند، منیزیوم به محیط های بین ستاره ای منتشر می شود و در آنجا می تواند در سیستم های جدید ستاره ای بازیافت شود.
منیزیم فلزی بسیار واکنش پذیر است و به صورت طبیعی فقط در ترکیب با عناصر دیگر به صورت کاتیون با ظرفیت +2 یافت می شود. بنابراین برای به دست آوردن آن به صورت خالص، باید آن را به صورت مصنوعی تولید کنیم.

در حال حاضر این فلز عمدتا از طریق الکترولیز نمک های منیزیم حاصل از شورابه (Brine) به دست می آید و در درجه اول به عنوان یک جزء اساسی در تولید آلیاژهای آلومینیوم – منیزیم کاربرد دارد. اهمیت منیزیوم به دلیل چگالی پایین نسبت به آلومینیوم است که در ترکیب با این فلز آلیاژهایی سبک و مستحکم تولید می کند. این آلیاژها با نام مگنالیوم یا مگنلیوم (magnalium or magnelium) شناخته می شوند.
منیزیم برای بدن ما انسان ها عنصری حیاتی محسوب می شود. این عنصر یازدهمین عنصر فراوان در بدن انسان است و برای ادامه زندگی همه سلول ها و حدود 300 آنزیم، ضروری است.
یون های منیزیم با ترکیبات پلی فسفاته مانندATP ، DNA و RNA واکنش می دهند. امروزه از ترکیبات منیزیوم به عنوان داروهای ملین، ضد اسیدها (مثلا شیر منیزیا) و تثبیت تحریکات عصبی غیر طبیعی یا اسپاسم رگ های خونی در شرایطی مانند اکلامپسی (eclampsia) استفاده می شود. برای درک اهمیت این عنصر برای بدن انسان، می توانید عبارت magnesium را در قسمت تصاویر گوگل سرچ کنید و نتایج را ببینید …
حقایقی جالب در خصوص فلز منیزیوم
- کلمه “منیزیم” از نام منطقه ای در یونان به نام مگنزیا برگرفته شده است. یکی از مکان هایی که ترکیبات این عنصر به طور طبیعی و فراوان وجود دارد.
- اگر کنجکاو شدید، بدانید “شیر منیزیا” چیست، بهتر است بدانید که به عنوان مُلَیِّن و برای درمان سوء هاضمه عمل می کند و ترکیبی از مولکول های منیزیم، هیدروژن و اکسیژن است.
- یون های منیزیوم مزه ای بسیار ترش دارند. مقدار اندکی از این فلز کافی است تا به یک بطری آب معدنی مزه ای ترش و زننده ببخشد.
- اضافه کردن آب به آتش حاصل از منیزیم، گاز هیدروژن تولید می کند که آتش را چندین برابر می کند.
- حدود 60 درصد منیزیم موجود در بدن انسان در اسکلت، 39 درصد در بافت های ماهیچه ای و یک درصد آن در فضای خارج سلولی وجود دارد.
- مصرف یا جذب کم منیزیم باعث دیابت، بیماری های قلبی، پوکی استخوان، اختلالات خواب و سندرم متابولیک می شود.
- منیزیوم اولین بار در سال 1755 توسط “جوزف بلک” به عنوان عنصر شناخته شد. با این حال، تا سال 1808 توسط “همفری دیوی” به طور خالص شناسایی نشد.
- چین تولید کننده اصلی منیزیم است که حدود 80 درصد از عرضه جهانی را به عهده دارد!
- منیزیم یون فلزی است که در مرکز هر مولکول کلروفیل گیاهی یافت می شود. بنابراین یک عنصر اساسی برای فتوسنتز است.
- ماده دارویی خانگی “نمک اپسوم” ترکیبی شامل سولفات منیزیم را دارد. نام “اپسوم” از چشمه ای در انگلستان می آید که نمک های منیزیم به طور طبیعی در آن یافت می شوند.
- طبق داده های USGS، ایالات متحده 65 تن منیزیم در ذخایر منیزیت طبیعی خود دارد. از این مقدار، 88 درصد آن در نوادا یافت می شود.
از کجا شروع شد؟!
در قسمت پیشین گفتیم که اولین نفری که عنصر منیزیوم را تشخیص داد، “جوزف بلک” در شهر ادینبورگ بود. او منیزیا (اکسید منیزیم، MgO) را از آهک (اکسید کلسیم CaO) تشخیص داد. اگر چه هر دو با گرمایش انواعی از سنگ های کربناته، منیزیت و سنگ آهک تولید شده بودند.
یکی دیگر از مواد معدنی منیزیم به نام Meerschaum (سیلیکات منیزیم) توسط “توماس هنری” در سال 1789 گزارش شد. وی در مقالاتش عنوان کرد که این ماده در ترکیه برای ساخت لوله های استعمال دخانیات بسیار استفاده می شود.
شکل ناخالص منیزیم فلزی اولین بار در سال 1792 توسط “آنتون روپراخت” تولید شد که منیزیا را با زغال چوب گرم می کرد. در نهایت مقدار خالص اما ناچیزی از این فلز در سال 1808 توسط همفری دیوی توسط الکترولیز اکسید منیزیم شناخته شد.
اما با تمام این تفاسیر، این دانشمند فرانسوی “آنتوان الكساندر بروتوس بُوسی” بود كه در سال 1831 با واکنش كلرید منیزیم با پتاسیم مقدار قابل توجهی از این فلز را سنتز نموده و سپس خواص آن را مطالعه كرد.

خواص فیزیکی منیزیم
منیزیم یک فلز نسبتاً سخت با ظاهری سفید-نقره ای است. در میان فلزات ساختاری (structural) منیزیم سبک ترین است. با این حال این فلز و آلیاژهای آن به اندازه ای قوی هستند که در ساخت ساختمان ها، پل ها ، اتومبیل و هواپیما مورد استفاده قرار گیرند.
در یک کلام، منیزیم به راحتی ساخته می شود! منظور ما از ساخت، شکل دادن، قالب گیری، خمش، برشکاری و هر نوع کار مکانیکی با این فلز است. اکثر فلزات سخت و شکل ناپذیر هستند. بنابراین باید به آلیاژ تبدیل شوند. این جا اهمیت منیزیوم پر رنگ می شود. این فلز که به راحتی ساخته می شود، می تواند با دیگر فلزات ترکیب شده و آلیاژهای منحصر به فردی تولید کند.
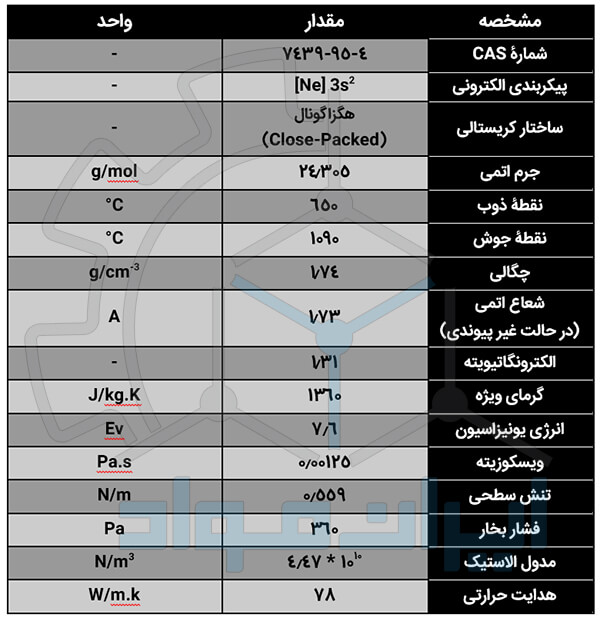
نقطه ذوب منیزیم 651 درجه سلسیوس (1200 درجه فارنهایت) و نقطۀ جوش آن 1100 درجۀ سلسیوس (2000 درجه فارنهایت) است. چگالی آن نیز 1.738 گرم بر سانتی متر مکعب است.
خواص شیمیایی منیزیم
این عنصر یک فلز نسبتاً فعال است. با آب سرد به آرامی و با آب گرم با سرعت بیشتری واکنش می دهد. در دمای اتاق با اکسیژن ترکیب شده و پوسته ای نازک از اکسید منیزیم ایجاد می کند. در دماهای بالا نیز با نور سفید کور کننده ای می سوزد.
منیزیوم با اکثر اسیدها و با برخی از مواد قلیایی واکنش می دهد. می دانیم که منظور از قلیایی، ماده ای شیمیایی با خاصیت مخالف اسید، یعنی بازی است. هیدروکسید سدیم و آب آهک نمونه هایی از مواد قلیایی هستند که منیزیم وارد واکنش با آن ها می شود.
این ماده همچنین به راحتی با بسیاری از غیر فلزات از جمله نیتروژن، گوگرد، فسفر، کلر، فلوئور، برم و ید ترکیب می شود. با تعدادی ترکیبات شناخته شده مانند مونوکسیدکربن، دی اکسید کربن، دی اکسید گوگرد و اکسید نیتریک به راحتی واکنش می دهد.
ایزوتوپ ها
منیزیم سه ایزوتوپ دارد که به طور طبیعی موجود هستند. منیزیم 24، منیزیم 25 و منیزیم 26. ایزوتوپ ها دو یا چند شکل از یک عنصر مشخص هستند که با توجه به عدد جرمی متفاوت از یکدیگر مجزا می شوند. عدد جرمی نیز نشان دهندۀ تعداد پروتون ها بعلاوۀ نوترون ها در هستۀ اتم عنصر است.
تعداد پروتون هاست که نوع عنصر را تعیین می کند. اما تعداد نوترون های موجود در اتم هر یک از عناصر می تواند متفاوت باشد. هر تغییر، نشان دهندۀ یک ایزوتوپ است. جالب است بدانید منیزیم یک ایزوتوپ رادیواکتیو یعنی منیزیم 28 نیز دارد. این ایزوتوپ هیچ استفادۀ مهم تجاری ندارد.
آلیاژهای منیزیم
اغلب آلیاژهای منیزیم از ترکیب این فلز با فلزاتی مانند آلومینیوم، روی، منگنز، سیلیسیم، مس، فلزات نایاب و زیرکونیم تولید می شوند. آلیاژهای منیزیم یک ساختار شبکه ای شش ضلعی هگزاگونال دارند که بر خواص بنیادی این آلیاژها تاثیر می گذارد.
تغییر شکل پلاستیک شبکه هگزاگونال پیچیده تر از فلزاتی با کریستال مکعبی مثل آلومینیوم، مس و فولاد است. بنابراین آلیاژهای منیزیم به طور معمول به عنوان آلیاژهای ریخته گری استفاده می شوند. این آلیاژها در بسیاری از اجزای اتومبیل های مدرن با عملکرد بالا استفاده شده اند.
نام آلیاژهای منیزیم اغلب با دو حرف و دو عدد مشخص می شوند. حروف، عناصر آلیاژی اصلی را معرفی می کنند (A = آلومینیوم، Z = روی، M = منگنز، S = silicon). اعداد نیز ترکیبات اسمی مربوطه عناصر آلیاژی اصلی را نشان می دهند. برای مثال علامت AZ91، آلیاژ منیزیم با حدود ۹ درصد آلومینیوم و ۱ درصد روی را نشان می دهد.
بررسی خوردگی در آلیاژها
وجود آهن، نیکل، مس و کبالت، به شدت خوردگی را در آلیاژهای منیزیم فعال می کند. در مقادیری بیشتر از حد آلیاژی معمول، این فلزات صورت ترکیبات بین فلزی رسوب می کنند و محل های رسوب به عنوان سایت های کاتدی فعال عمل می کنند. این سایت ها آب را احیا کرده و باعث از دست رفتن منیزیم می شوند.
بدیهی است که با کنترل مقدار این فلزات مقاومت در برابر خوردگی را می توان تا حدود زیادی بهبود بخشید. وجود منگنز کافی می تواند بر اثرات خورنده آهن در این آلیاژها غلبه کند. همچنین افزودن ماده ای کاتدی، هیدروژن اتمی را در ساختار فلز می گیرد.
با به کارگیری این تکنیک، از تشکیل گاز هیدروژن آزاد، یک عامل اساسی در فرآیندهای شیمیایی خورنده جلوگیری می شود. همچنین افزودن حدود 1 در 300 قسمت آرسنیک، خوردگی را در محلول نمک با فاکتوری نزدیک به ده کاهش می دهد.
تا بحث های متالورژیکی داغ است، کمی هم از خزش حرف بزنیم! تحقیقات نشان داده است که تمایل منیزیم به خزش در دماهای بالا با افزودن عناصر اسکاندیم و گادولینیوم از بین می رود. اشتعال پذیری با مقدار کمی کلسیم در آلیاژ بسیار کاهش می یابد.

منیزیم در طبیعت
حدود 2.1 درصد از پوسته زمین از منیزیم تشکیل شده است. همین امر آن را به هشتمین (یا در برخی منابع ششمین) عنصر فراوان در زمین تبدیل می کند. البته منیزیم به شکل طبیعی در آب دریا نیز وجود دارد. جالب است بدانید یک مایل مکعب آب دریا، حاوی حداکثر شش میلیون تن منیزیم است!
این عنصر در بسیاری از مواد معدنی طبیعی حضور دارد. از مهم ترین آن ها می توان دولومیت، منیزیت یا کربنات منیزیم (MgCO3)؛ کارنالیت یا پتاسیم منیزیم کلرید (KMgCl3) و اپسومیت یا سولفات منیزیم (MgSO4) را نام برد.
بزرگترین تولید کننده سنگ های معدنی منیزیم ترکیه است. دیگر تولیدکنندگان بزرگ کره شمالی، چین، اسلواکی، اتریش و روسیه هستند. مقدار منیزیم تولید شده در ایالات متحده به منظور محافظت از اسرار تجاری گزارش نشده است.

منیزیم تولید شده در ایالات متحده از سه منبع آب دریا، شوراب ها و معادن تأمین می شود. آب دریا به منظور به دست آوردن منیزیم توسط شرکت هایی در کالیفرنیا، دلاور، فلوریدا و تگزاس فرآوری می شود. همچنین این عنصر از شوراب ها در میشیگان و یوتا نیز به دست می آید. شورابه (brine) آبی است که حتی از آب دریا شورتر است.
در سال های اخیر تقاضای جهانی برای منیزیم مخصوصا در صنایع خودروسازی و صنایع تولید آلیاژهای آلومینیومی رشد چشمگیری داشته است. همچنین گسترش صنایع تولید فولاد و آلومینیوم در کشورهای حاشیه خلیج فارس و استفاده از منیزیم به عنوان عامل گوگردزا در صنایع فولاد، افزایش تقاضا برای منیزیم در کشورهای منطقه را به دنبال داشته است. پیش بینی می شود تا سال 2025 میزان تقاضای این فلز در دنیا به بالای یک میلیون و 200 هزار تن در سال برسد.
ایران به قطب منیزیم در جهان تبدیل می شود؟!
به گزارش پایگاه خبری “عصر معدن” و به نقل از ایرنا، ظرفیت های ایران در کنار دیگر کشورهای تولید کننده فلز منیزیم قابل توجه است. از این رو امکان توسعه این صنعت در برخی استان های کشور مانند خراسان جنوبی، اصفهان، آذربایجان شرقی و غربی، همدان، کرمانشاه، فارس و کرمان وجود دارد.
این در حالی است که منیزیم فلز آینده دنیا نامیده می شود و کشورهای اروپایی این فلز را در لیست مواد خام و فلزات استراتژیک اتحادیه اروپا قرار داده اند. این فلز به دلیل سبکی و دارا بودن خواص مکانیکی و مقاومت حرارتی مطلوب، جایگزین فلزات رایج کاربردی مانند فولاد، چدن و آلومینیوم به شمار می رود.
کشور ما به علت دارا بودن منابع معدنی، انرژی عظیم و موقعیت ژئوپلیتیکی مناسب در جهان، قادر است به عنوان یکی از قطب های مهم صنایع انرژی در خاورمیانه و جهان تبدیل شود. حرکت از خام فروشی به سمت تولید محصولات با ارزش افزوده بالا و صادرات محور باعث وارد شدن ایران به لیست کشورهای تولید کننده محصولات استراتژیکی چون منیزیم و آلیاژهای آن خواهد شد.
سنگ معدن اصلی منیزیم در ایران، منیزیت است. معادن منیزیت معمولا در شرق ایران مرتبط با توده های اولترابازیک غنی از منیزیم هستند و به اشکال رگه ای، گل کلمی و لایه ای تشکیل شده اند. معدن “سربیشه” در خراسان جنوبی یکی از مهمترین معادن منیزیت در ایران است که سالانه 32 هزار تن منیزیت از این معدن استخراج می شود.

فرایند استخراج منیزیوم
متداول ترین فرایند تولید منیزیم که در چین از آن استفاده می شود، فرایند سیلیکوترمیک است. در این فرایند، اکسیدهای موجود، در دماهای بالا در حضور سیلیکون احیا می شوند. این فرایند معمولا با استفاده از فروسیلیکون ها انجام می گیرد. البته این فرایند را می توان در حضور کربن و در دمای 2300 درجه سلسیوس نیز اجرا کرد. واکنش های تولید منیزیم با این روش را در ادامه مشاهده می کنید.
اما در آمریکا داستان کمی متفاوت است. در آمریکا منیزیم تحت فرایندی به نام DAW استخراج می شود. در فرایند DAW منیزیم کلرید به دست آمده از شورابه ها یا دریاها به صورت گداخته درآمده و الکترولیز می شود.
پس از این فرایند، یک محلول نمکی شامل یون Mg2+ به دست می آید که با افزودن اکسید کلسیوم به آن، منیزیم هیدروکسید رسوب می کند. سپس با استفاده از هیدروکلریک اسید و گرمایش محلول و الکترولیز، منیزیم خالص به دست می آید.
ترکیبات و کاربردها
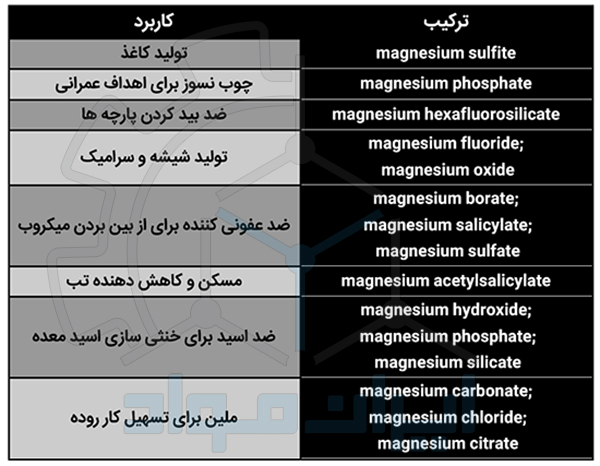
پیش از این که به کاربردهای عمومی منیزیم اشاره کنیم، بهتر است چند ترکیب مهم این عنصر که سبب شهرت بیشتر منیزیم شده اند را در جدول زیر ببینیم.
منیزیم و نقش های بایولوژیکی
پیش از این گفتیم که منیزیم بخشی از کلروفیل گیاهان است. رنگدانه ای سبز که گیاهان برای استخراج انرژی از نور خورشید استفاده می کنند. گیاهانی که منیزیم کافی ندارند، نمی توانند کلروفیل کافی تولید کنند. در نتیجه برگ های آنها لکه هایی مایل به زرد ایجاد می کند.
طبق تحقیق کتابخانه ملی پزشکی ایالات متحده، این عنصر برای بیش از 300 فرآیند بیولوژیکی در بدن انسان بسیار مهم است. زنان بزرگسال باید حدود 320 میلی گرم منیزیم در روز و مردان بزرگسال 420 میلی گرم منیزیم مصرف کنند.
میوه ها، سبزیجات، آجیل، حبوبات و غلات کامل منابع خوبی از این عنصر هستند. پزشکان گاهی مکمل های منیزیم را برای انواع شرایط پزشکی از جمله فشار خون بالا، سندرم قبل از قاعدگی و دیابت توصیه می کنند.
افراد الکلی و کودکان در کشورهای فقیر معمولا دچار کمبود منیزیم می شوند. در چنین مواردی، کمبود منیزیم ممکن است باعث شود فرد به راحتی ناراحت یا پرخاشگر شود. از طرف دیگر، قرار گرفتن بیش از حد در معرض منیزیم نیز مشکل ساز است.
به عنوان مثال، استنشاق پودر منیزیم می تواند باعث تحریک گلو و چشم شود و در نتیجه تب ایجاد کند. در دوزهای زیاد، منیزیم می تواند به عضلات و اعصاب آسیب برساند و یا حتی در مواردی منجر به از دست دادن احساس و فلج شود.

و اما کاربردهای منیزیوم به عنوان فلز!
صنایع متالورژی
کاربردهای اصلی فلز منیزیم در این حوزه عبارتند از:
- آلیاژسازی با مشارکت فلز آلومینیوم
- ریخته گری دایکست (به صورت آلیاژ با روی)
- تولید تیتانیوم در فرآیند کرول (Kroll)
- حذف گوگرد در فرایندهای تولید آهن و فولاد
از این عنصر برای ایجاد گرافیت گره ای (nodular) در آهن ریختگی استفاده می شود. همچنین می توان از آن به عنوان آند گالوانیکی (فداشونده) در لوله ها، قایق ها و هیترهای آب بهره جست. امروزه باتری های منیزیومی یکی از موارد قابل سرمایه گذاری برای تولید باتری های قابل شارژ به شمار می روند.
در سال های اخیر از این عنصر در تولید مواد و آلیاژهای فوق العاده مستحکم و سبک وزن استفاده می شود. به عنوان مثال، وقتی منیزیم با نانوذرات کاربید سیلیکون ترکیب شود، از استحکام ویژه بسیار بالایی برخوردار خواهد شد. کاربرد قابل ذکر دیگر، استخراج اورانیم و دیگر فلزات از نمک هایشان است.
صنایع هوافضا
از نظر تاریخی، منیزیم یکی از اصلی ترین فلزات در صنایع هوافضا بود و برای ساخت هواپیماهای ارتش آلمان از اوایل جنگ جهانی اول و به طور گسترده ای برای هواپیماهای آلمانی در جنگ جهانی دوم استفاده می شد. تا آن جا که آلمانی ها آلیاژی به نام Elektron از این عنصر ابداع کردند. اصطلاحی که امروزه نیز استفاده می شود.
در صنایع تجاری هوافضا، به دلیل خطرات ناشی از آتش سوزی و خوردگی، از این عنصر در اجزای مربوط به موتور استفاده نمی شود. البته به دلیل اهمیت صرفه جویی در مصرف سوخت، امروزه استفاده از آلیاژهای منیزیم در صنایع هوافضا در حال افزایش است.
اخبار حاکی از آن است که آلیاژ Elektrom 21 خواص مناسبی برای استفاده در موتورها، چارچوب کلی و دیگر بخش های داخلی هواپیما از خود نشان داده است. البته فعلا در مرحله تست!
صنایع اتومبیل سازی
در سال های پیشین، مرسدس بنز از آلیاژ Elektron در بدنه مدل اولیه مرسدس بنز 300 SLR استفاده كرد. این اتومبیل ها در مسابقات قهرمانی Sportscar World 1955 شرکت کردند که سبب فاجعه معروف LeMans شدند. سوختن قسمت هایی از آلیاژ Elektron باعث این حادثه بود.
کمپانی پورشه از فریم های آلیاژ منیزیم در اتومبیل 917/053 که در سال 1971 برنده مسابقه لمانز شد، استفاده کرد. این سری اتومبیل ها به دلیل برتری از لحاظ وزن، همچنان از آلیاژهای منیزیم برای بلوک های موتور خود استفاده می کنند.
گروه مشهور “فولکس واگن” نیز سال هاست که در اجزای موتور خود از آلیاژهای این عنصر استفاده می کند. کمپانی بیامدابلیو نیز از معرکه عقب نمانده است. این شرکت در موتور N52 از آلیاژ منیزیم استفاده کرده است. البته این موتور شامل آلیاژهای آلومینیوم برای دیواره های سیلندر و پوشش های خنک کننده است که توسط آلیاژی از منیزیم با نام AJ62A احاطه شده است.
این موتور بین سال های 2005 و 2011 در سراسر جهان در مدل های مختلف BMW سری 1، 3، 5، 6 و 7 و همچنین Z4 ، X1، X3 و X5 مورد استفاده قرار گرفت. کمپانی شورولت نیز از آلیاژ منیزیم AE44 در مدل Corvette Z06 2006 استفاده کرد.

صنایع الکترونیک
به دلیل چگالی کم و خواص مکانیکی و الکتریکی مطلوب، از منیزیم به طور گسترده ای برای تولید تلفن های همراه، رایانه های شخصی و تبلت، دوربین ها و سایر قطعات الکترونیکی استفاده می شود. برای ایجاد فلش در دوربین های عکاسی نیز می توان از این عنصر بهره جست.
خطر این فلز را جدی بگیرید!
فلز منیزیم و آلیاژهای آن می توانند خطرات انفجاری داشته باشند. علی رغم کاربردهایی که انواع ایمن آن در آتش بازی ها دارند، در صورتی تکه ای از این عنصر به صورت پودر یا روبان و به شکل خالص بسوزد، بسیار قابل اشتعال است.
فراموش نکنید که منیزیم مذاب یا در حال سوختن، به شدت با آب واکنش نشان می دهد. سوختن منیزیم با استفاده از خاموش كننده شیمیایی خشک كلاس D و یا پوشاندن آتش آن با ماسه قابل رفع است.
هنگام کار با پودر منیزیم، از عینک های ایمنی با قابلیت محافظت کامل از چشم و فیلترهای UV استفاده کنید. چرا که سوختن منیزیم سبب تولید نور ماورای بنفش می شود که به شبکیه چشم انسان آسیب می رساند.
برای دریافت فایل ها با گوشی همراه، دکمه دانلود را برای چند لحظه فشرده و در یک صفحه جدید فایل مربوطه را دانلود نمایید.
پسورد فایل فشرده : www.iran-mavad.com



















دیدگاه کاربران