 جدید
جدیدکربن و آلوتروپ های آن (Carbon)
کربن عنصری غیر فلزی و فراوان است که با نماد C و عدد اتمی ۶، در گروه ۴ اصلی و ردیف ۲ در جدول تناوبی قرار دارد. این عنصر در بدن تمامی موجودات زنده یافت می شود. این عنصر دگرشکل های مختلفی دارد که بیشتر آن ها ساخته دست بشر هستند و هر کدام در جای خود کاربرد مخصوصی دارند.

کربن به عنوان یک غیر فلز در بسیاری از علوم مهندسی جای خود را باز کرده است. این عنصر نافلز در عین این که پایه شیمی آلی را تشکیل می دهد، در بسیاری از علوم پایه و مهندسی نظیر مهندسی مواد، مهندسی نفت و حتی مهندسی مکانیک نقش مهمی را بازی می کند. همان طور که در ادامه خواهیم دید، بخشی از پیشرفت صنعت متالورژی و نانو مواد مدیون کربن و دگرشکل های آن است.
در این ویدئوی کوتاه توجه شما را به معرفی این عنصر جذاب جلب می کنیم.
دگرشکل های کربن
کربن در انواع مختلف میکروسکوپی وجود دارد که در این بخش به معرفی، بیان خواص و کاربرد آن خواهیم پرداخت.
گرافیت (Graphite)
گرافیت یکی از دگرشکلهای کربن و پایدارترین آنها است. این دگرشکل کربن معمولا در ساختار شش وجهی یا هگزاگونال متبلور میشود، به شکل طبیعی از معادن استخراج می شود و یا به منظور کاربردهای خاصی سنتز می شود.
گرافیت ساختار لایه لایه دارد به طوری که هر لایه از کنار هم قرار گرفتن اتمهای کربن با پیوند کوالانس شکل میگیرند این لایهها با پیوند ضعیف واندروالس بر روی هم قرار گرفتهاند که با اعمال کوچکترین نیرویی این پیوندها شکسته می شوند. همین موضوع سبب می شود که گرافیت مغز مداد به سادگی روی کاغذ جاری شود.
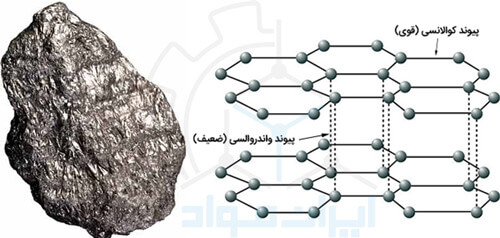
ویژگی های گرافیت
- مقاومت در برابر خوردگی
- مقاومت حرارتی بالا تا ۲۵۰۰ درجه سانتی گراد
- رسانایی الکتریکی و حرارتی بالا
- مقاومت شیمیایی بالا
- مقاومت فشاری بالا
- اصطکاک پایین
کاربردهای گرافیت
دیرگدازها: به دلیل رسانایی حرارتی گرافیت و همچنین بالا بودن نقطه ذوب و پایداری حرارتی و شیمیایی، از آن در ساخت بوتههای نسوز، نازلها، استوپرها و همچنین دیرگداز های منیزیا- کربن، آلومینا-گرافیت و… استفاده میشود.

باتریها: گرافیت های طبیعی و مصنوعی به دلیل هدایت بالای الکتریکی به عنوان مادهی اولیهی الکترود در صنعت باتری سازی کاربرد دارند.
فولادسازی: گرافیت در در فولادسازی جهت تامین کربن مورد نیاز برای ساخت فولادهای مختلف و همچنین به عنوان روانکننده در دهانه ی اکسترودر جهت اکسترود کردن فولاد کاربرد دارد.
لنت ترمز: گرافیت آمورف و ریزدانه طبیعی به دلیل پایداری حرارتی، اصطکاک کم و … به عنوان لنت ترمز در خودروهای سنگین کاربرد دارد.
مداد: به دلیل ساختار لایه لایه و نرم گرافیت و امکان اثرگذاری بر صفحهی کاغذ، به عنوان مغزی مداد استفاده میشود.
الماس (Diamond)
الماس یکی از مهمترین دگرشکلهای کربن بعد از گرافیت است که در ساختار چهار وجهی یا مکعبی متبلور میشود. الماس دارای پیوندهای بسیار قوی کوالانت است لذا به عنوان سخت ترین ماده در طبیعت شناخته میشود.
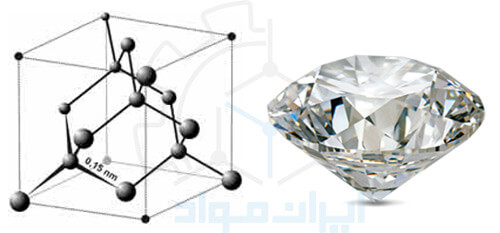
خواص الماس
سختی بالا: الماس سختترین ماده در طبیعت است.
چقرمگی: چقرمگی الماس طبیعی MPa · m1 / 2 10-5/7 اندازه گیری شده است. این مقدار در مقایسه با سایر مواد سرامیکی خوب است، اما در مقایسه با بیشتر مواد مهندسی مانند آلیاژهای مهندسی، که به طور معمول دارای سختیهایی بیش از MPa · m1 / 2 100 هستند، ضعیف است.
استحکام فوق العاده: الماس استحکام تسلیم فشاری حدود GPa 130-140 دارد که در مقایسه با بسیاری از سرامیکها عدد بسیار بالایی است.
خواص الاستیک: معمولاً تلاش برای تغییر شکل بلور الماس بالک با تست کشش یا تست خمش منجر به شکست ترد میشود. با این حال، هنگامی که الماس تک کریستالی به شکل سیم یا سوزن به اندازه نانومتر است (قطر ۱۰۰- ۳۰۰ نانومتر)، می توان آنها را به اندازه ۹ درصد کرنش پلاستیک بدون شکست، تحت کشش قرار داد.
خواص الکتریکی: برخی از الماس های آبی برخلاف اکثر الماسها، نیمههادیهای عالی هستند. رسانایی و رنگ آبی ناشی از ناخالصی بور است.
هدایت حرارتی: در دمای محیط هدایت حرارتی الماس از تمامی مواد بالاتر و ۵ برابر بیشتر از مس است.
خواص سطحی: الماس به طور طبیعی آبگریز است، به این معنی که سطح الماس را نمیتوان با آب مرطوب کرد، اما به راحتی توسط روغن مرطوب می شود.
پایداری شیمیایی: در دمای اتاق، الماس با هیچ ماده شیمیایی از جمله اسیدهای قوی و پایه واکنش نمی دهد اما الماس در جو اکسیژن خالص و از دمای ۶۹۰ تا ۸۴۰ درجه سانتیگراد میسوزد.
کاربردهای الماس
- از الماس به دلیل سختی و مقاومت فشاری بالا در سنبههای تست سختی سنجی استفاده میشود.
- کاربرد دیگر آن به دلیل پایداری و انتقال حرارت بسیار بالا، سختی و مقاومت فشاری بالا در متههای حفاری چاههای نفت است .
- در صنایع مختلف مثل صنعت شیشه از الماس جهت ابزار برش استفاده میکنند.
- کاربرد به عنوان سلولهای سندان الماس (DAC) (ابزاری برای شبیهسازی فشار در آزمایشهای هوافضا برای ساخت رباتهای سیارهپیما، فضاپیماها و … است).
- به دلیل قابلیت عبور تقریبا تمام طیفهای نوری، در تولید قطعات اپتیکی از الماس اسفاده میشود.
گرافن (Graphene)
گرافن یکی دیگر از دگرشکلهای کربن است که به دلیل خواص منحصر به فردی که دارد، در سال های اخیر سر و صدای زیادی به پا کرده است. گرافن یک لایه دو بعدی از اتمهای کربن است که در آن اتم ها با پیوند کوالانسی به هم متصل شده اند. هر اتم با سه پیوند کوالانسی به اتم های کربن دیگر متصل شده و باعث ایجاد یک ساختار لانه زنبوری شده است. از اتصال لایه های گرافن با پیوند ضعیف واندروالس، گرافیت تشکیل می شود.

خواص گرافن
- لایههای گرافن در برابر کشش بسیار قوی هستند و خیلی راحت خم میشوند، اما پاره نمیشوند.
- گرافن به طور قابل توجهی رسانای خوب برق و گرما است.
- دانسیته بالا و ضریب عبور نوری خوب از دیگر ویژگی های گرافن است.
کاربردهای گرافن
- ساخت بدنههای با وزن پایینتر مثل بدنه هواپیما و ماهواره
- استفاده از گرافن در ساخت ابرخازن و ترانزیستور
- رساناسازی پلاستیکها با جاسازی گرافن
- بالابردن دوام باتریها
- ساخت پوششهای شفاف و رسانا در سلولهای خورشیدی و نمایشگرها
- افزایش استحکام و دوام ایمپلنت های پزشکی
- استفاده در ساخت تجهیزات ورزشی
- استفاده در صفحات لمسی و نمایشگرها
فولرن (Fullerene)
فولرن یا باکیبال یک آلوتروپ مرموز کربن است که مولکولهای آن از اتمهای کربن متصل شده توسط پیوندهای منفرد و دوتایی تشکیل شده است. به طوری که می تواند مش بسته یا نیمه بسته را تشکیل دهد، این مولکول ممکن است یک کره توخالی، بیضی، لوله یا بسیاری از اشکال و اندازههای دیگر باشد.
نحوهی نامگذاری باکیبالها به شکل نوشتن C به نمایندگی از نام کربن و یک عدد در جلوی آن به نمایندگی از تعداد اتمها در هر توپ است. مثال C60، C70 و…

خواص فولرن
- استحکام مکانیکی: اساساً استحکام فشاری و تنش تسلیم در فولرن بسیار بالاست به طوری که اگر تا ۳۰۰۰ اتمسفر به آن فشار وارد شود دوباره به حالت اولیه خود بازمیگردد.
- خاصیت روانسازی بالا: به دلیل پیوندهای ضعیف واندروالس بین مولکولهای فولرن، این مولکولها به هم چسبیدهاند و در عین حال قابلیت لغزش بر روی یکدیگر را دارند.
- حساسیت به نور: فولرن در برابر نور بسیار حساس است. به این ترتیب که با تغییر در طول موج تابیده شده خواص الکتریکی آن به شدت تغییر میکند.
- ساختار توخالی: وجود فضاهای خالی در وسط هر مولکول فولرن، موقعیت مناسبی جهت قرارگیری اتم، یون و دسته اتم است که باعث بهبود خواص مختلف آن میشود.
- خواص زیست سازگاری: همین فضاهای خالی نیز موقعیت مناسبی برای قرارگیری برخی از داروها، هورمونها و آنزیمها جهت استفاده در نانو پزشکی است.
کاربردهای فولرن
- کاربرد به عنوان نانو کامپوزیت جهت افزایش تنش تسلیم در فاز زمینه کامپوزیت
- جایگزینی فولرن جهت روانساز در صنایع مختلف به جای گرافیت
- کاربرد در سلول خورشیدی به دلیل حساسیت به نور
- کاربردهای نانوپزشکی و درمان بیماریها (در جدیدترین دستاورد، درمان ویروس ایدز با فولرن) و ساخت دستگاههای MRI به دلیل فضای توخالی
- استفاده به عنوان کاهنده های نوری، سنسور های مبتنی بر فولرن، سیم یا قفس مولکولی
نانو لوله کربنی (Carbon Nano Tube)
نانولولههای کربنی (Carbon Nanotubes یا CNTs) لوله هایی هستند که از کربن ساخته شده اند و معمولا قطری در حد ابعاد نانو دارند. این آلوتروپ کربن که خواص و کاربردهای منحصر به فردی دارد، دارای ساختاری یکپارچه با شبکه شش وجهی است. می توان گفت نانو لوله کربنی دقیقا ساختاری شبیه لایههای گرافیت (گرافن) دارد.
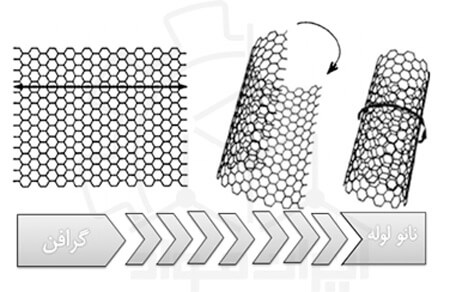
انواع نانولوله کربنی
نانولولههای کربنی چند دیواره
نانولولههای کربنی چند دیواره را میتوان از لایههای متعددی گرافنی ساخت که معمولا با حفرهای با قطر ۲ تا ۲۵ نانومتر بهصورت متحدالمرکز با فاصله ۳۴/۰ نانومتر از هم جدا شدهاند.
نانولولههای کربنی تک دیواره
نانولوله کربنی تک دیواره حاصل پیچیدن یک لایه گرافن به دور خودش است که یک استوانه با قطر ۲ – ۱ نانومتر را ایجاد کرده است.

خواص نانولوله های کربنی
- خواص مکانیکی: نانولولههای کربنی یکی از مستحکم ترین مواد مهندسی بهشمار میرود. مدول الاستیک، استحکام شکست و استحکام خمشی بهطور شگفت انگیزی بالا، گواهی بر این موضوع است. انرژی کرنشی بالا نیز باعث ایجاد امکان ذخیره و جذب انرژی زیاد در این ماده شدهاست.
- هدایت الکتریکی: نانولولهکربنی با توجه به ساختار، قطر و تغییر خواص میتواند ابر رسانا، رسانا و یا نیمههادی باشد.
- انتقال بالستیک: انتقال بالستیک یعنی حرکت الکرونها در طول یک رسانا بدون پراکندگی و هدر رفت انرژی. انتقال الکتریسیته در در طول نانولولهها به طور طبیعی بالستیک است.
- هدایت حرارتی بالا، چگالی سطحی بالا، سطح جداره صاف، گسیل و جذب نور، ممان مغناطیسی بسیار بزرگ، حساسیت به تغییرات کوچک نیروهای اعمال شده و تولید ولتاژ از دیگر خواص این ماده است.
کاربردهای نانو لوله های کربنی
با توجه به خواص یاد شده میتوان از کاربردهای این ماده در ترانزیستورها، حسگرها، استحکام دهی کامپوزیتها، صنایع هوا و فضا، ذخیره سازی گازها و… اشاره کرد.
کربن سیاه (Carbon black)
کربن سیاه آلوتروپ آمورف (بی شکل) کربن است که بهصورت تجاری از تجزیه حرارتی و اکسایشی هیدروکربنها ساخته میشود. نام گذاری انواع کربن سیاه نیز بر اساس همین فرایند تولید آن انجام می شود. مثلا؛ کربن سیاه تولید شده به روش احتراق جزئی گاز طبیعی را Channel Blacks مینامند.

خواص کربن سیاه
- نسبت سطح به حجم بالا
- جذب اشعه ماوراء بنفش
- رسانایی الکتریسیته خوب
کاربردهای کربن سیاه
- حدودا ۷۰% کربن سیاه تولیدی به عنوان رنگدانه و تقویت کننده در لاستیک های خودرو استفاده می شود. کربن سیاه به انتقال گرما از سطح آج و کمربند لاستیک کمک میکند و با این کار باعث کاهش آسیب حرارتی و افزایش عمر تایر میشود.
- حدود ۲۰٪ از تولیدات جهانی کربن سیاه به تسمه، شیلنگ و سایر محصولات لاستیکی تعلق میگیرد.
- بخشی از کربن سیاه تولیدی به عنوان رنگدانه در جوهرها، روکشها و پلاستیکها استفاده میشود. به عنوان مثال، اضافه کردن کربن سیاه به پلی پروپیلن باعث جذب اشعه UV می شود و از تخریب پلیمر جلوگیری می کند.
- ذرات کربن سیاه در برخی موارد به عنوان جاذب رادار در تونرهای فتوکپی و لیزر پرینتر استفاده میشوند.
- در کامپوزیت سازی، از کربن سیاه به عنوان فاز تقویت کننده در پلاستیک، الاستومر ، فیلمها، چسبها و رنگها استفاده می شود.
- از کربن سیاه به عنوان یک ماده افزودنی ضد الکتریسیته ساکن در محفظه و لولههای سوخت خودرو استفاده می شود.
منابع
اصغری بیاتی؛ یونس. آشنایی با نانولولههای کربنی . دانشگاه تربیت دبیر شهید رجایی
برای دریافت فایل ها با گوشی همراه، دکمه دانلود را برای چند لحظه فشرده و در یک صفحه جدید فایل مربوطه را دانلود نمایید.
پسورد فایل فشرده : www.iran-mavad.com












دیدگاه کاربران