
خوردگی گالوانیک (خوردگی دوفلزی)
مفهوم خوردگی گالوانیک
زمانی که دو فلز متفاوت در یک الکترولیت تماس الکتریکی داشته باشند، از فلز نجیبتر محافظت بیشتری میشود و فلز فعالتر تمایل بیشتری به خوردگی دارد. در این حالت نوعی آسیب خوردگی رخ میدهد که به آن خوردگی گالوانیک گفته میشود.
بهطورکلی برای ایجاد خوردگی گالوانیک، سه شرط باید وجود داشته باشد:
- فلزات از لحاظ الکتروشیمیایی مشابه نباشند.
- فلزات باید در تماس الکتریکی باشند.
- فلزات باید در معرض الکترولیت قرار بگیرند.
این نوع خوردگی معمولاً با عناوین خوردگی دوفلزی (Bimetallic Corrosion) و خوردگی فلزات نامشابه (Dissimilar Metal Corrosion) نیز شناخته میشود. موارد زیر برخی از عوامل مؤثر بر میزان خوردگی گالوانیک هستند:
- اختلاف پتانسیل الکتریکی بین مواد
- کارایی کاتد
- نواحی سطحی میان مواد متصل
- مقاومت الکتریکی اتصال میان مواد و الکترولیت

خوردگی دوفلزی بر چه اساسی ایجاد می شود؟
فلزات و آلیاژهای فلزی همگی دارای مقادیر مختلفی از پتانسیل الکترود (Electrode Potential) هستند. این پتانسیل، نوعی معیار نسبی از تمایل فلز به فعال شدن در یک الکترولیت معین است. هر چقدر فلز دارای فعالیت بیشتر یا نجابت کمتری باشد، احتمال تشکیل آند از آن در محیط الکترولیتی بیشتر است. درحالیکه فلز هرچه نجیبتر باشد، احتمال ایجاد کاتد بیشتر است.
الکترولیت بهعنوان مجرایی برای انتقال یونها عمل میکند و یونهای فلزی را از آند به کاتد منتقل میکند. در نتیجه، فلز آند با سرعت بیشتری تحت فرسایش قرار میگیرد. درحالیکه فلز کاتد با سرعت کمتری خورده میشود و در بعضی موارد، ممکن است اصلاً خورده نشود.
در این راستا یک سری گالوانیک بررسی شده در آب دریا وجود دارد که فلزات رایج را به ترتیب از آندیترین (فعالترین) تا کاتدیترین (نجیبترین) ذکر کرده است. هرچه فاصلۀ دو فلز در این فهرست از یکدیگر بیشتر باشد، سرعت خوردگی گالوانیک بیشتر خواهد بود.
بهعنوانمثال، روی در اثر تماس با پلاتین بهسرعت در آبنمک خورده میشود. اما فولاد ضدزنگ 304 در تماس با فولاد ضدزنگ 316 تأثیر کمی از لحاظ خوردگی گالوانیک بر روی یکدیگر خواهند داشت.

سری گالوانیک، راهنمای کاربردی برای مهندسین
سری گالوانیک یک راهنمای بسیار کاربردی برای مهندسان است. همانطور که گفتیم، موقعیت دو فلز یا آلیاژ در سری گالوانیک، میزان خوردگی دوفلزی را تعیین میکند. بهعنوانمثال، آلومینیوم و مس را در نظر بگیرید. از جدول میتوان مشاهده کرد که آلومینیوم در سری گالوانیک نسبت به مس فعالتر است و بنابراین میتواند بهعنوان آند عمل کند. مس نیز به دلیل موقعیت نسبتاً نجیبتر به کاتد تبدیل میشود.
مس : نخستین فلز کشف شده به دست بشر!
اگر تمام سیم های مسی به کار گرفته در یک اتوموبیل معمولی را از آن خارج کنید و به ...معمولاً اتصال فلزات و آلیاژهای نزدیک به هم در سری گالوانیک باعث خوردگی دوفلزی نمیشود، چرا که هر چه مواد سری گالوانیک به هم نزدیکتر باشند، اختلاف پتانسیل (نیروی محرکۀ خوردگی) کمتر است.

چه عواملی باعث خوردگی گالوانیک میشوند؟
همانطور که گفتیم، خوردگی گالوانیک یک فرایند الکتروشیمیایی است. بهعبارتدیگر، این آسیب در نتیجۀ گردش جریانهای الکتریکی بسیار کوچک بین دو فلز غیر مشابه رخ میدهد که باعث خوردگی بیشتر آند و کمتر تحت تأثیر قرار گرفتن کاتد میشود.
جریان الکتریکی به دلیل اختلاف پتانسیلی که بین دو قطعۀ فلزی یا بین قسمتهای مختلف یک فلز وجود دارد، جریان مییابد. درحالیکه الکترولیت (مثلاً یک رطوبت جزئی) در نقطۀ تماس وجود دارد.
نیاز به وجود رطوبت در طی فرسایش با این واقعیت بیان میشود که در آب و هوای بسیار خشک، بهعنوانمثال در مناطق خاصی از هند و آفریقا، اتصالات آهنی با قدمت بسیار زیادی هنوز بدون آسیب باقی ماندهاند. از آنجا که بخش اعظم خوردگی از فرایند اکسیداسیون تشکیل میشود، وجود یک منبع اکسیژن ثابت در سطح فلز برای ایجاد خوردگی لازم است.
حتی اگر تماس واقعی وجود نداشته باشد، در صورت وجود الکترولیت ممکن است این نوع اتصال ایجاد شود. مثلاً در برخی موارد ممکن است فلز نجیبتر کمی خورده شود و در آبی حل شود که متعاقباً از فلز فعال عبور کند. در این حالت، فلز نجیبتر بر روی فلز فعالتر رسوب میکند و از این طریق یک تماس دوفلزی واقعی ایجاد میشود.
در ادامه هریک از عوامل مؤثر بر خوردگی گالوانیک را به تفکیک بررسی میکنیم.
اختلاف پتانسیل
هرچه اختلاف پتانسیل بین دو فلز بیشتر باشد، مقدار خوردگی دوفلزی نیز بیشتر است. یک مثال صنعتی از این اتفاق، خوردگی دریچۀ لولۀ چگالش (Condensate Pipe) است (تصویر زیر).
در این مثال، دریچۀ چدنی درون لولۀ چگالش از جنس فولاد ضدزنگ AISI 304 گذاشته شده است. این سیستم در کنار یک مبدل حرارتی از مس قرار داده شد. اختلاف پتانسیل بین مس، فولاد و چدن باعث خوردگی دوفلزی و تخریب قطعه شده است.

رسوب ناخالصیها
رسوب ناخالصیها در اغلب سازههای صنعتی غیرمجاز است. رسوب ناخالصیها باعث تشکیل سیستمهایی تحت عنوان سلولهای هوادهی افتراقی (Differential Aeration Cells) میشود. تشکیل این سلولها موجب جذب رطوبت از هوا و در نهایت خوردگی گالوانیک میشود.

سطح غیرفعال فولاد ممکن است توسط چنین رسوباتی از بین برود. از این طریق که مکانهای زیر رسوبات بهعنوان آند عمل میکنند و منجر به حفره میشوند. اینجا اهمیت یک طراحی خوب مشخص میشود که نباید اجازه ایجاد ناخالصی روی سطح را بدهد. مثلاً در اتومبیلها اجزا باید طوری طراحی شوند که احتباس آب در سطح را به حداقل برسانند.

اتمسفر مرطوب
پیش از این نیز گفتیم که اگر سطح مرطوب باشد، بهویژه اگر ذرات نمک در رطوبت وجود داشته باشد، خوردگی گالوانیک تشدید میشود. طراحی اجزا نباید موجب باقی ماندن لایة آب روی سطح شود. یک سطح صیقلی و صاف اجازۀ احتباس آب را نمیدهد. طراحی سطحی صاف که به سمت پایین متمایل است، اجازه نمیدهد لایۀ مرطوب برای مدت زمان بیشتری باقی بماند.
تماس با مواد عایق مرطوب
تماس با مواد عایق مانند پشم شیشه، الیاف شیشه و فوم پلیاورتان تا زمانی که مواد عایق خشک باشند، باعث خوردگی فولاد در تماس با عایقها نمیشود. بهطورکلی عوامل زیر منجر به خوردگی ناشی از عایق میشوند:
- نفوذ رطوبت در عایق و در نتیجه تجزیۀ نمکهای محلول با pH کم (حدود 2-3)
- ایجاد یونهای کلرید
- از بین رفتن انفعال فولاد توسط یونهای کلرید و شروع ایجاد حفرات
- چرخههای آبوهوایی (مانند چرخههای «خشک-مرطوب» و «خشک- گرم و مرطوب»)
- موانع رطوبت ناکافی (مثلاً فاصلۀ نامناسب عایق)
یک طرح ایدهآل برای جلوگیری از خوردگی ناشی از عایق در شکل زیر نشان داده شده است.
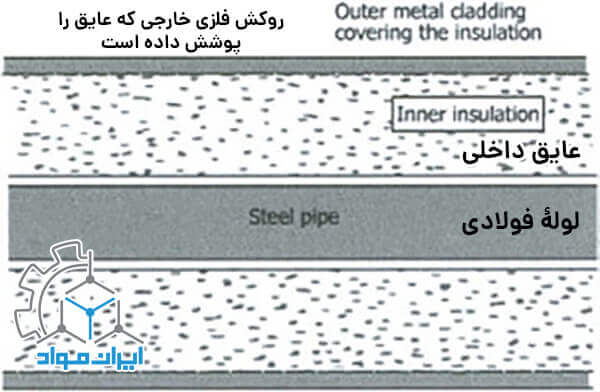
نسبت آند به کاتد
یک ناحیۀ آندی کوچک در کنار یک ناحیۀ کاتدی بزرگ، باعث خوردگی دوفلزی جدی میشود. زیرا چگالی جریان زیادی در یک ناحیۀ آندی کوچکتر ایجاد میشود.
چگونه می توان شدت خوردگی گالوانیک را کنترل کرد؟
شدت خوردگی دوفلزی به پتانسیل فلزات درگیر، سطح نسبی آنها و رسانایی الکترولیت موجود بستگی دارد. معمولاً سطح خوردگی دوفلزی در محیط غوطهور بیشتر از محیط جوی خواهد بود. بهعنوانمثال، در یک محیط جوی اگر نسبت سطح فلزات آندی و کاتدی کم باشد، شدت خوردگی گالوانیک کم خواهد بود یا اگر پارامتر فرکانس یا دورۀ رطوبت (Period Of Dampness) (بهعنوانمثال وجود یک الکترولیت) کم باشد، میزان خوردگی دوفلزی کم خواهد بود.
برعکس، اگر فلزات مختلف در یک الکترولیت قویتر مانند آب دریا غوطهور شوند، سطح خوردگی دوفلزی به طور قابلتوجهی بیشتر خواهد بود. به همین ترتیب، غوطهوری در آب شیرین (که رسانایی کمتری دارد) تأثیر قابلتوجهتری نسبت به قرار گرفتن در معرض جو خواهد داشت.
راهکارهایی جهت محدود کردن خوردگی دوفازی
اصول اساسی برای جلوگیری از خوردگی گالوانیک عبارتاند از:
راهکار اول: استفاده از یک مادۀ عایق بین فلزات غیرمشابه بهگونهای که در تماس مستقیم الکتریکی نباشند. این راهکار به شکل مؤثری مدار الکتریکی را میشکند.
راهکار دوم: جلوگیری از پل زدن (Bridging) الکترولیت میان دو فلز
راهکار اول در صورتی قابل اجراست که در شرایط غوطهوری، به دلیل نیاز به برقراری اتصال الکتریکی بین دو فلز، مجبور به برداشتن عایق نباشیم. راهکار دوم نیز با اعمال رنگ یا پوشش های آلی در قسمتی از فلز که در شرایط غوطه وری قرار دارد، حاصل می شود. در مواردی که محافظت از این طریق دنبال میشود، اگر پوشاندن هر دو فلز غیرممکن باشد، ترجیح بر این است که فلز نجیبتر پوششدهی شود. ترکیبات اتصال باید بتوانند به طور کامل جلوی آب را بگیرند. همچنین نباید خشک شوند، ترک بخورند یا خودشان تحت خوردگی قرار بگیرند.
آیا خوردگی دوفلزی می تواند فوایدی داشته باشد؟
خوردگی دوفلزی در مواردی میتواند مفید باشد. پتانسیل و جریانی که بین فلزات غیرمشابه وجود دارد، در سنسورها برای سنجش پارامتر مدتزمان رطوبت (Time Of Wetness) در آزمون خوردگی جوی استفاده میشود.
نگاهی بر انواع تست های خوردگی
تست های خوردگی از قدرتمندترین ابزارهای ارزیابی کیفیت مواد به شمار می روند. این ...هنگامیکه آب باران یا شبنم بر روی سنسور وجود دارد، یک جفت گالوانیک ایجاد میشود، درحالیکه در صورت عدم رطوبت زوج گالوانیک فعال نیست. سنسورهای مشابه را میتوان در داخل اتصالات لببهلب (Lap Joints) یا سایر مناطقی که دسترسی به آنها سخت است دفن کرد. از این روش، میتوان برای تعیین وجود رطوبت کافی برای ایجاد خوردگی در جایی که دیده نمیشود، استفاده کرد.
در این راستا، مواد ویژهای که میتوانند جریانهای خوردگی گالوانیک بالایی ایجاد کنند، بهصورت پودر تهیه می شوند. هنگام خیس شدن، این پودرها منجر به سرعت بسیار بالای خوردگی میشوند که در نتیجۀ این پدیده، گرمای قابلتوجهی تولید میشود.
جالب است بدانید از همین طریق است که وعدههای غذایی آماده (Meals Ready To Eat) یا بهاختصار MRE برای نیروهای مسلح ایالات متحده تولید میشود. فقط کافی است آب اضافه کنید تا یک وعدۀ غذایی گرم داشته باشید.
خوردگی گالوانیک اساس کار اکثر باتریها نیز هست. جریانی که توسط زوج گالوانیک درون باتری تولید میشود، سالهاست در اسباببازیها، تلفنهای همراه و سایر سختافزارهای الکترونیکی استفاده میشود.
جمعبندی
در این مقاله تلاش کردیم تا با زبانی ساده، شما را با مفاهیم اساسی خوردگی گالوانیک آشنا کنیم. زمانی که دو فلز یا آلیاژ مختلف در معرض رطوبت در کنار هم قرار می گیرند، هر کدام پتانسیل خاصی جهت خوردگی ایجاد می کنند و تحت این شرایط فلز نجیب تر به کاتد و فلز فعال تر به آند تبدیل می شوند. بنابراین فلز فعال تر با خورده شدن، از فلز نجیب تر محافظت می کند. توجه به این موضوع، مهندسین را مجاب می کند که از مزایای خوردگی گالوانیک برای حفاظت مواد ارزشمند استفاده کنند (برای مثال پوشش دهی فولادهای کربنی با استفاده از فلز روی). اما در مجموع عدم توجه و کنترل این نوع از خوردگی می تواند خسارت های جبران ناپذیری به صنایع وارد کند.
در پایان یک ویدئوی آموزشی از یک ارائه دانشگاهی به زبان انگلیسی برای دانلود در اختیار شما قرار داده شده است. این ویدئو درباره خوردگی گالوانیک و راه های پیشگیری از آن به طور مفصل بحث می کند.
برای دریافت فایل ها با گوشی همراه، دکمه دانلود را برای چند لحظه فشرده و در یک صفحه جدید فایل مربوطه را دانلود نمایید.
پسورد فایل فشرده : www.iran-mavad.com












دیدگاه کاربران